神經醯胺是近年來當紅的保濕成分,不分大廠小廠、國內國外的保養品牌紛紛推出含有神經醯胺的產品。保濕是一年四季都不該忽略的重要保養關鍵,也常有許多保濕迷思流傳在坊間,值得大家好好了解。近年來市場上當紅的幾種保濕成分中,除了上次討論過的角鯊之外,大概就是神經醯胺了。網路上可以找到不少文章在介紹神經醯胺的在異位性皮膚炎或濕疹相關疾病的功能與應用,但內容的正確性不一,因此 MedPartner 團隊回顧了大量文獻,在這邊幫大家做個詳細的整理與更新,除了由淺入深的介紹之外,也對市面上含神經醯胺的產品做了個調查,希望大家在購買相關的產品時能多一分思考,找到自己最適合的保養品喔!
神經醯胺(Ceramide)與類神經醯胺(Pseudoceramide)是什麼?
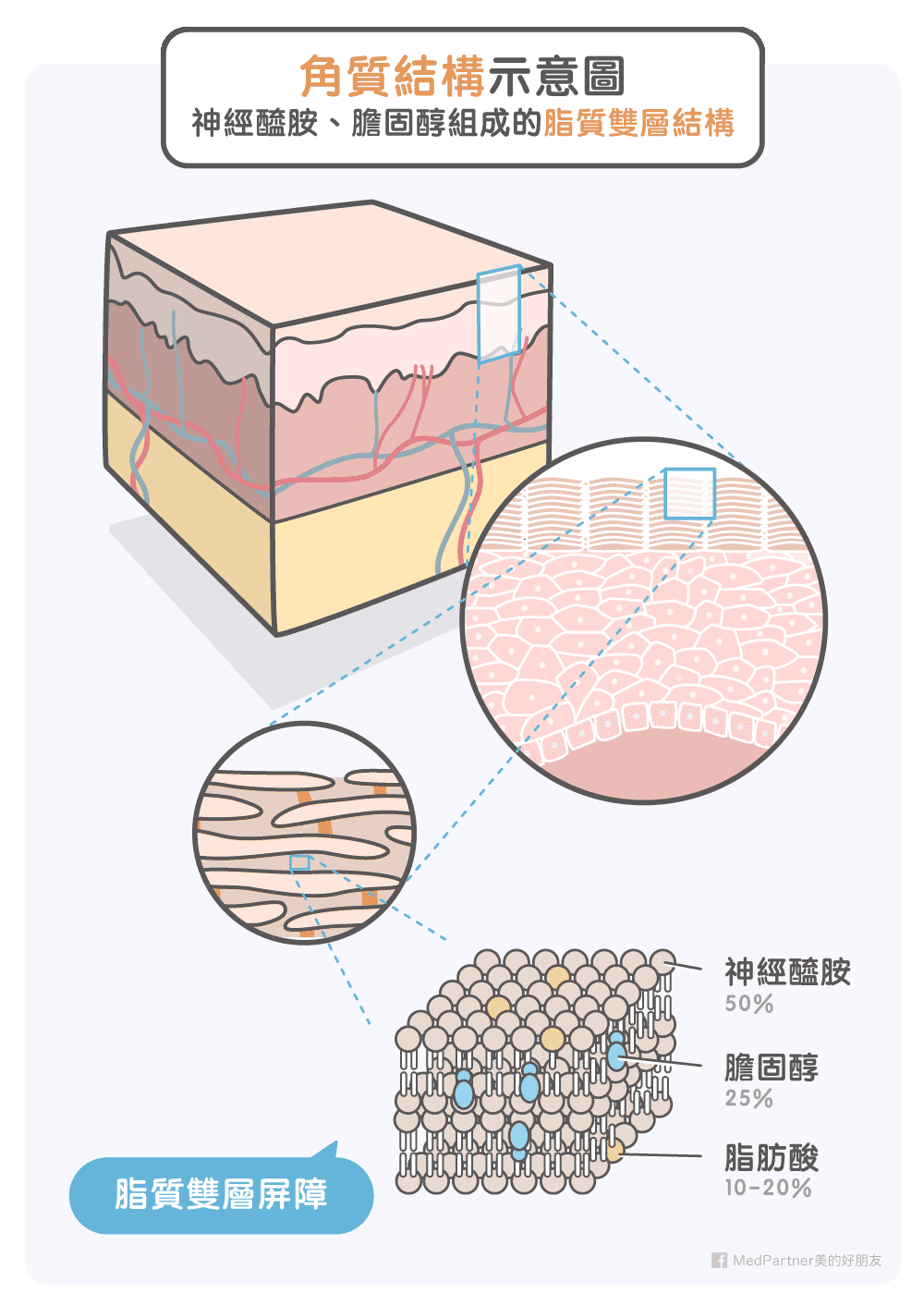
神經醯胺(Ceramide)又名分子釘或賽洛美,為角質層細胞間脂質的主要成分,占比約 50%,神經醯胺的結構組成是很複雜的,皮膚中神經醯胺約有 300 多至 1000 種的變化。由於其同時具有親水與親油的特性,所以能夠形成脂質雙層的結構,加了間質的柔軟度與保水能力。人體皮膚的神經醯胺也會隨著時間而流失,而造成雙脂質層的結構紊亂,進而使肌膚屏障的能力下降。
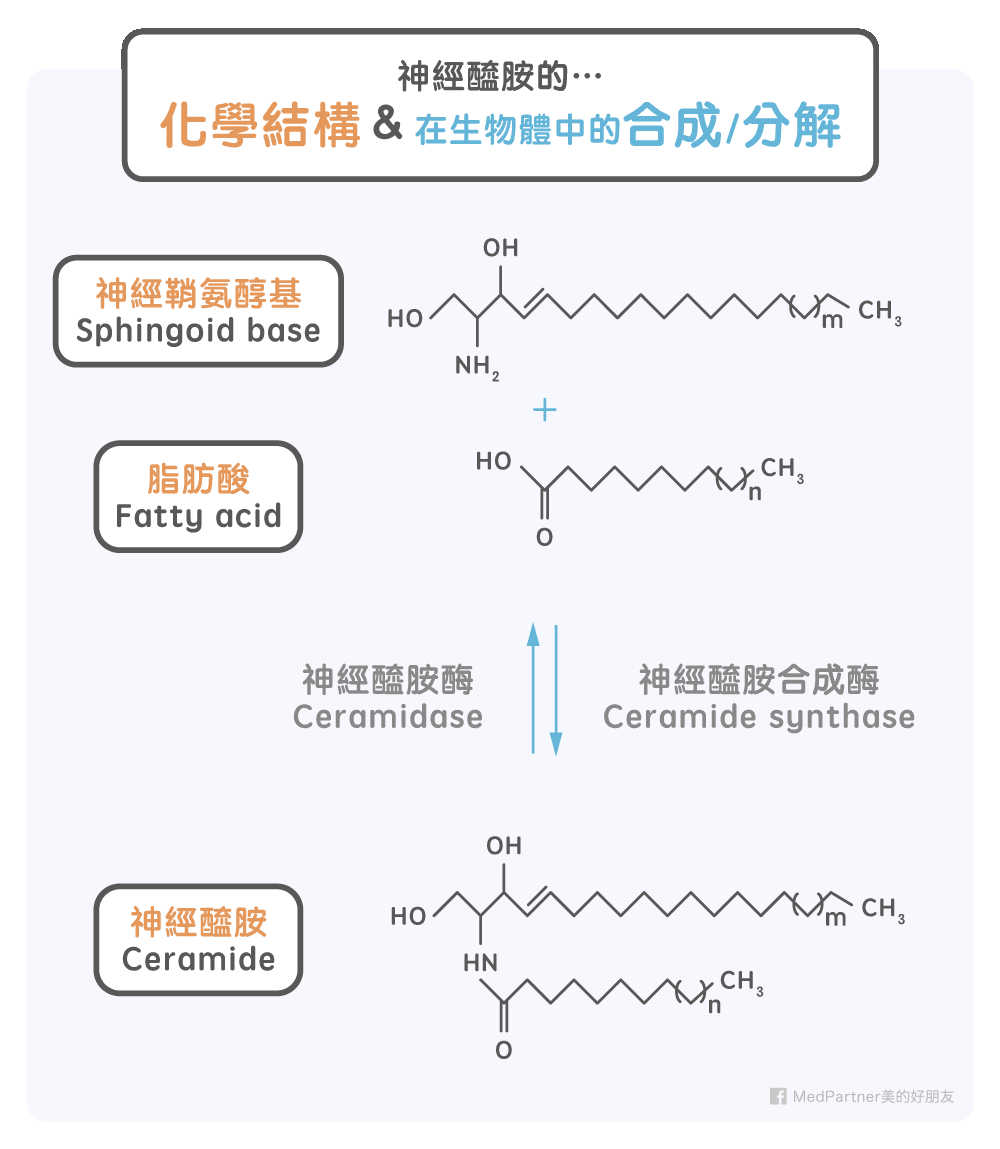
神經醯胺(Ceramide)又名分子釘或賽洛美,為角質層細胞間脂質的主要成分,占比約 50%,與膽固醇(25%)跟脂肪酸(10~20 %)共同組成重要的皮膚屏障 [Ref.1]。神經醯胺的基本結構是由神經鞘氨醇基(Sphingoid base)及脂肪酸(Fatty acid)所形成,藉由神經醯胺合成酶與神經醯胺酶進行合成與分解。神經醯胺同時具有親水與親油的特性,所以能夠形成脂質雙層的結構 [Ref.2]。至今有一些研究模型來解釋它的脂質雙層排列方式,較廣為接受且實驗數據充足的脂質雙層模型為神經醯胺具有方向性的排列,且以膽固醇穿插其中。這樣的排列使得各脂質雙層間充滿著碳氫化合物間的作用力,增加了間質的柔軟度與保水能力。
到目前為止有數十種游離性神經醯胺被發現 [Ref.3],這樣的分類是根據神經鞘氨醇基及脂肪酸上的官能基不同所做的區分,神經鞘氨醇基上的官能基變化有 S、P、H、T、DS 命名,脂肪酸上的官能基變化則有 N、A、O、E 命名。例如 Ceramide [NP] 是由無羥基團脂肪酸(Non-hydroxy fatty acid, N)與植物鞘氨醇(Phytosphingosine, P)所組成。這些命名的方式與大家所熟悉的 Ceramide 1、Ceramide 3 等命名大不相同,由於以羅馬數字作為代號失去了科學上的辨識基準,所以舊的 INCI 命名方法已在 2014 年之後陸續淘汰 [Ref.4],不過市場上目前仍然是新舊並存的情況。
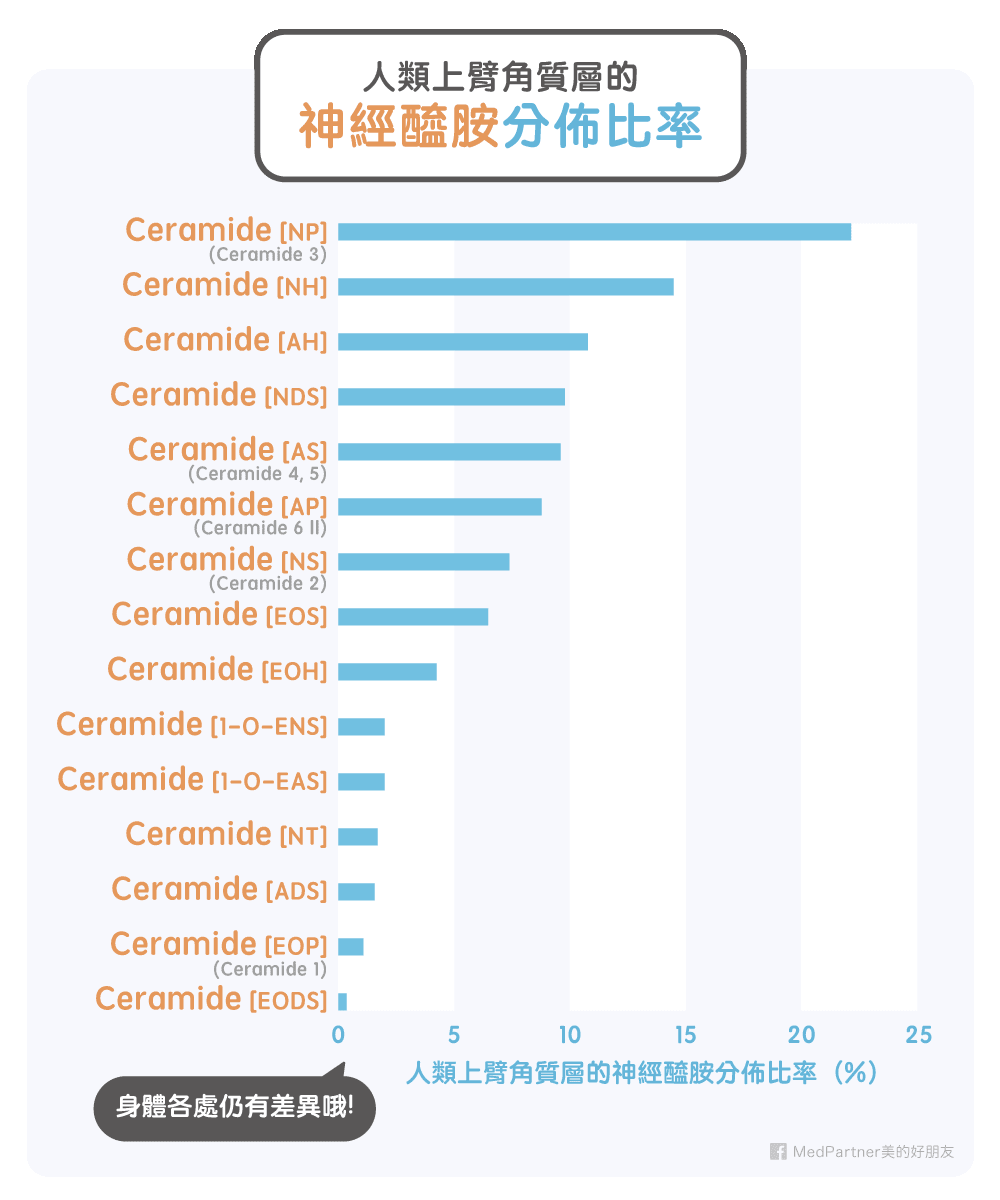
有研究以健康的成年人的上臂肌膚來分析神經醯胺的組成 [Ref.5],結果以 Ceramide [NP] 的 22% 為最多,其次是 Ceramide [NH] 的 14.5%,最少的 Ceramide [EODS] 不到 1%。這個粗估的結果可以告訴我們神經醯胺在皮膚結構中的複雜性,另外也需要注意的是人體各個部位皮膚的神經醯胺組成比例是會不同的喔。除了官能基的不同造成的神經醯胺複雜性,神經鞘氨醇基及脂肪酸的碳鏈長度也不是固定的,其兩個鏈的總碳數小至約 20 個碳,大的可至 70 個碳。這樣的碳長鏈差異可以使得神經醯胺有 300 多至 1000 種的變化。而據分析,人體角質層中大於 40 個碳總數的神經醯胺約占 88 % [Ref.6]。人體皮膚的神經醯胺也會隨著時間而流失,而造成雙脂質層的結構紊亂,進而使肌膚屏障的能力下降 [Ref.7-8]。

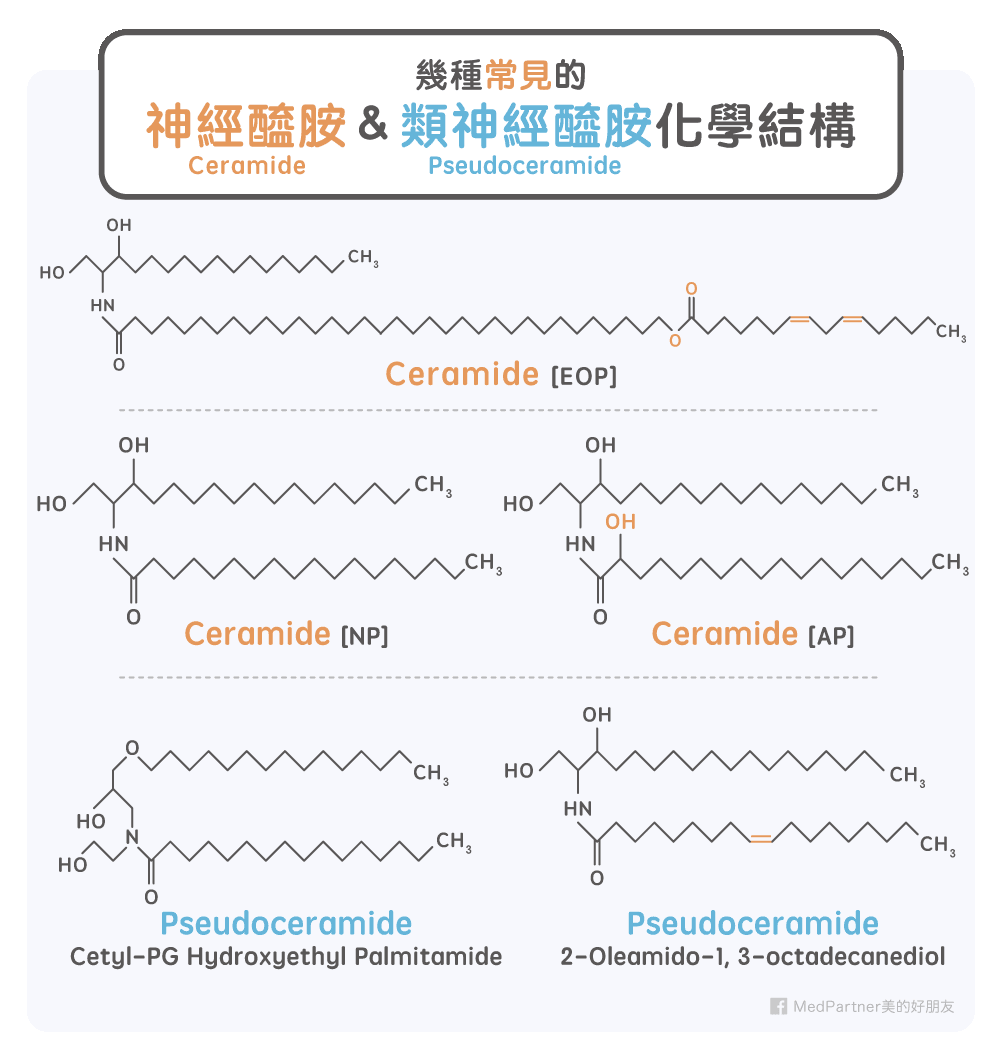
大部分的神經醯胺以人工合成為主,目前可以合成的有 6 種,少部分則來自植物萃取。除了天然神經醯胺之外,也有以人工合成的類神經醯胺(Pseudoceramide),它具有與神經醯胺相似的結構,也同樣具有親水與親油的特性。其餘兩類物質(Sphingolipids、Glycosphingolipids)有比例難以掌握、成分功能性與 ceramides 有所區別的問題,結構上應具保濕能力,但臨床研究不如 ceramides 和 pseudoceramides 充足。
從上述的介紹來看,神經醯胺確實是皮膚中很重要的一個成分,所以適當的補充神經醯胺似乎是有益的。以來源來說,大部分的神經醯胺以人工合成為主,目前可以合成的有 6 種,少部分則來自植物萃取。但是無論來源,只要確保該結構與人體中的神經醯胺一樣且經過分離純化去除其他物質,使用起來就不會有安全的疑慮。除了天然神經醯胺之外,也有以人工合成的類神經醯胺(pseudoceramide),它具有與神經醯胺相似的結構,為兩個碳氫長鏈以醯胺鍵鍵結,也同樣具有親水與親油的特性,理論上來說是可以形成脂質雙層的構造。常見的類神經醯胺有 Cetyl-PG Hydroxyethyl Palmitamide、2-Oleamido-1,3-Octadecanediol、Hydroxypalmitoyl sphinganine,此三種是市面上最常見的類神經醯胺添加物,其餘還有 Hydroxylauroyl Phytosphingosine、Hydroxycaproyl Phytosphingosine、Hydroxycapryloyl Phytosphingosine、Caproyl Sphingosine、Caprooyl Sphingosine、Caprooyl Phytosphingosine 等。值得注意的一點是,有些產品會標榜添加神經醯胺,而實際添加的為 Sphingolipids(鞘磷脂),此為神經鞘氨醇基及其衍生物組成的混合物,混合物包括了神經醯胺以及不含脂肪酸的單鍊神經鞘氨醇基衍生物(碳數約為20)。它的來源可以是哺乳類動物、酵母菌以及植物,只不過其中神經醯胺的含量與組成隨著來源不同也會有很大的差異。另外一種 Glycosphingolipids(醣神經胺醇脂)為神經醯胺親水端鍵結一個或多個醣基的物質,多存在於較角質層更內層的顆粒細胞層(Granular cells),由於此類脂質特性較為親水,所以它的功能必然與神經醯胺有所區別。小結,上述這兩類物質(Sphingolipids、Glycosphingolipids)從組成結構來看是具有保濕功能的,但是臨床實驗上的研究不若神經醯胺與類神經醯胺這麼的充足。(比例難以掌握、其他成分功能性與 ceramides 有所區別,其他成分結構上應具保濕能力,但臨床研究不如 ceramides 和 pseudoceramides 充足)
神經醯胺(Ceramide)與類神經醯胺(Pseudo-Ceramide)的外用保養功效如何?
神經醯胺在細胞生長、分化、老化過程中是重要的訊號傳導因子,甚至近年有應用神經醯胺研究抗癌的可能性。神經醯胺除了和皮膚保養有關以外,與多種皮膚疾病也相關。在某些疾病中,可發現特定種類的神經醯胺下降的變化,但在其他疾病中卻可發現某些種類的神經醯胺上升伴隨其他種類神經醯胺下降的情形。更複雜的還包括某些種類神經醯胺的碳鏈長短出現變化。以異位性皮膚炎(Atopic dermatitis)的情況而言,數種神經醯胺增加而數種神經醯胺減少,碳鏈的長度也有增有減。適當補充神經醯胺可能對某些皮膚疾病有幫助。但神經醯胺在皮膚疾病上的變化,大多可能只是結果,不是成因,單純補充神經醯胺可能可以改善症狀但是無法根治。
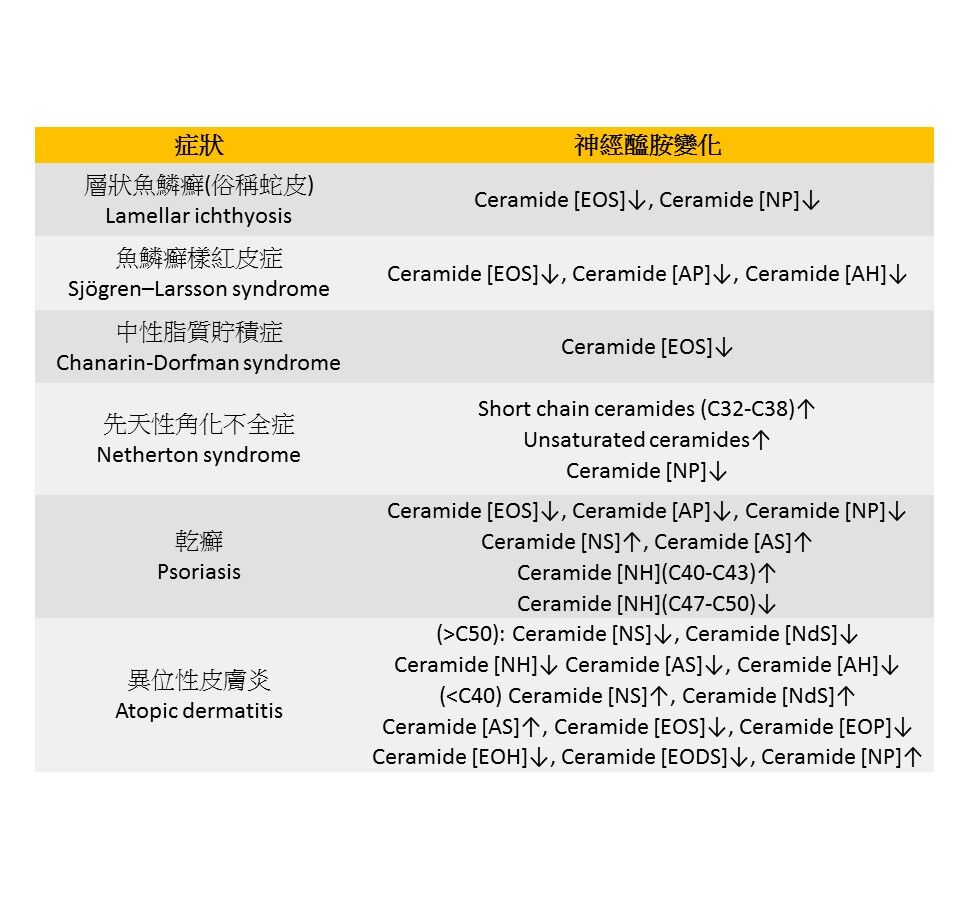
神經醯胺的功能有很多,它在細胞生長、分化、細胞凋亡等過程中屬於重要的訊號傳導因子,近年來有些研究應用神經醯胺來探討抗癌的可能性 [Ref.9]。在這邊我們只會著重在皮膚保養上的功效介紹。神經醯胺變化與很多皮膚疾病相關 [Ref.3],例如在層狀魚鱗癬(Lamellar ichthyosis)病人中有兩種神經醯胺 Ceramide [EOS] 跟 Ceramide [NP],被發現顯著的降低。但並不是所有的皮膚疾病伴隨的都是神經醯胺數量的下降,在乾癬症狀(Psoriasis)裡Ceramide [NS] 跟 Ceramide [AS] 則是上升的情況,更複雜的情形是除了各種 Ceramide 的數量增減,單一類型的Ceramide 碳數的多寡也會改變,例如短鏈 Ceramide [NH] (C40-C43) 為上升而長鏈 Ceramide [NH] (C47-C50) 為減少的情況。目前研究最多的異位性皮膚炎(Atopic dermatitis)有更複雜的情況,數種神經醯胺增加而數種神經醯胺減少,碳鏈的長度也有增有減。這些皮膚疾病伴隨著的神經醯胺變化必然導致雙脂質層的結構紊亂,而喪失了皮膚屏障原來該有的功能。理論上,若能適時適量的補充失去的神經醯胺應該可以改善受損的皮膚狀況。但是我們要思考的是神經醯胺在皮膚疾病上的變化大多只是果而不是因,例如魚鱗癬樣紅皮症(Sjögren–Larsson syndrome)是因為脂肪醛去氫酶基因(ALDH3A2)突變而造成的,單純補充神經醯胺可能可以改善症狀但是無法根治。
下面為較為複雜的臨床研究討論,我們先做個小結論:神經醯胺與類神經醯胺的濃度不一定是決定功效的關鍵因素,可能需有其他適當的添加物以及最適化的比例才能發揮功效。大部分的研究指出含仿角質層脂質(膽固醇、脂肪酸)的神經醯胺混合物可以增加皮膚的含水量,而達到修復受損皮膚的功效。另外,這些研究著重在對受損的肌膚修復研究(先天或後天),對於健康肌膚的日常保養而言,能夠提供多大的益處則是值得思考的問題。
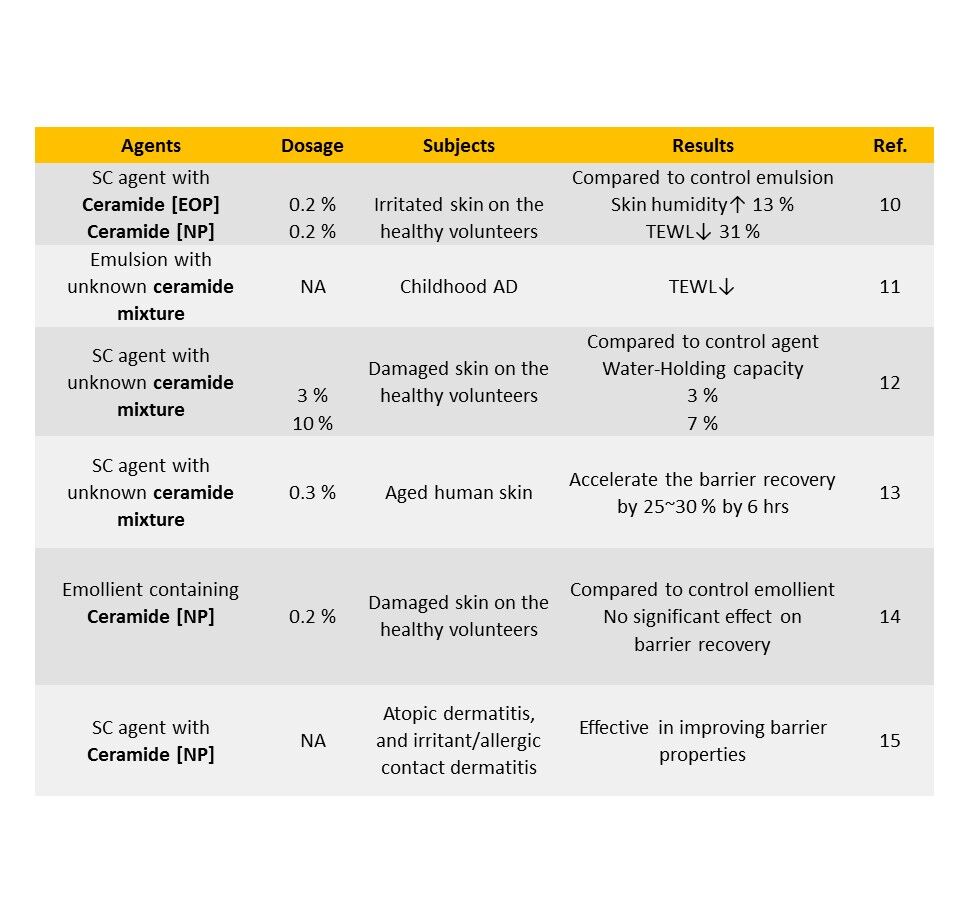
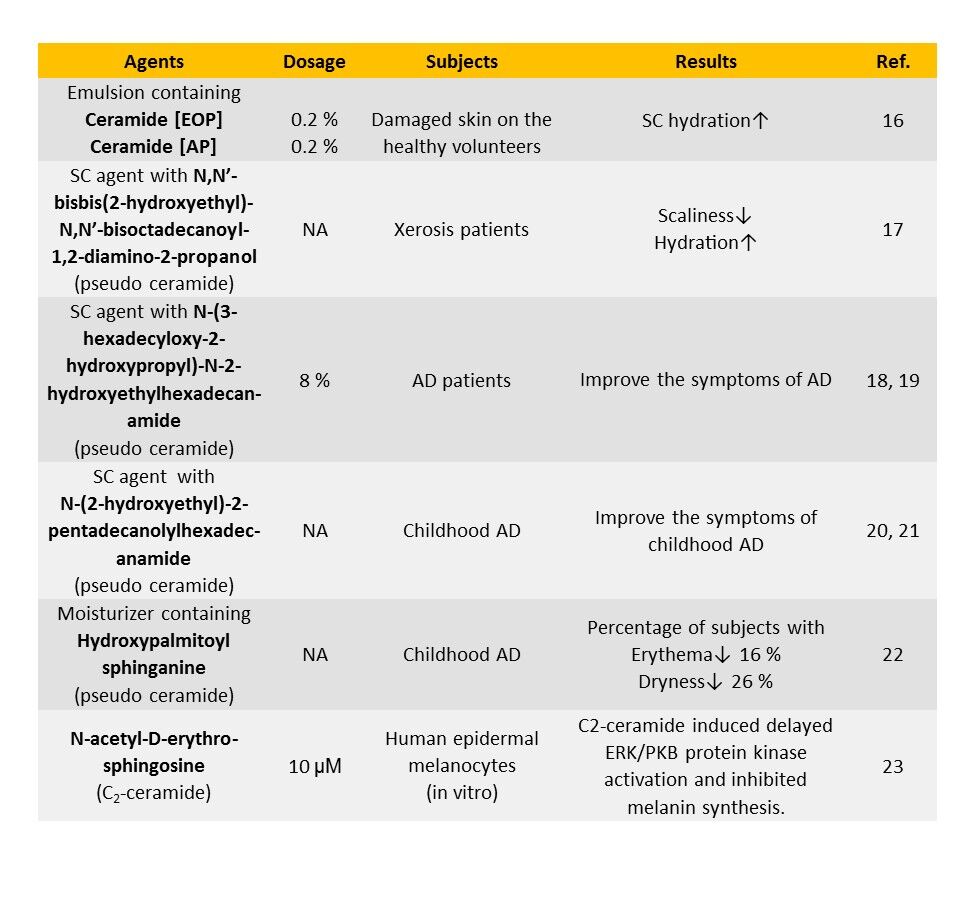
以神經醯胺與類神經醯胺在臨床上的研究來看,現階段在改善異位性皮膚炎的症狀以及後天受損的肌膚上有比較多的探討。下表為較詳細的臨床結果整理供專業人士與業界人士參考。這些研究使用的神經醯胺濃度分布在 0.2 % ~ 10 %,不論使用量的多寡,均有研究證明神經醯胺的添加可以增加皮膚的保水度及減少經皮水分散失。有趣的是,有一份研究使用了含 0.2 % Ceramide [NP] 的潤滑乳液,在受損的肌膚上測試,其結果跟控制組(使用不含 Ceramide [NP] 的潤滑乳液)相比並沒有顯著的差異 [Ref.14]。另一份研究同樣使用了含 Ceramide [NP] 的潤滑乳液,差異在於其使用的配方含有膽固醇與脂肪酸等仿角質層脂質混合物,但是卻可以觀察到對皮膚屏障的改善 [Ref.15]。另外,文獻中有使用多種神經醯胺的混合物,但是大部分並沒有清楚的標示使用種類以及比例如何,因此增加了解多重神經醯胺配方效果的難度。類神經醯胺方面的研究也指出其可以改善肌膚狀況增加保水度,但是使用的有效添加量不是很明確。在美白功效方面,有研究使用 N-acetyl-D-erythro-sphingosine(C2-ceramide)這一種神經醯胺,其為脂肪酸鏈為兩個碳的短鏈構造,在體外培養之人體表皮黑色素細胞(Human epidermal melanocytes)進行實驗,結果顯示此種神經醯胺可以延遲 ERK/PKB 蛋白激酶的活化,進而影響酪氨酸酶(Tyrosinase)的表現,而達到美白的功效 [Ref.23]。
台灣市面上含神經醯胺保養品的情況?消費者該如何選擇?
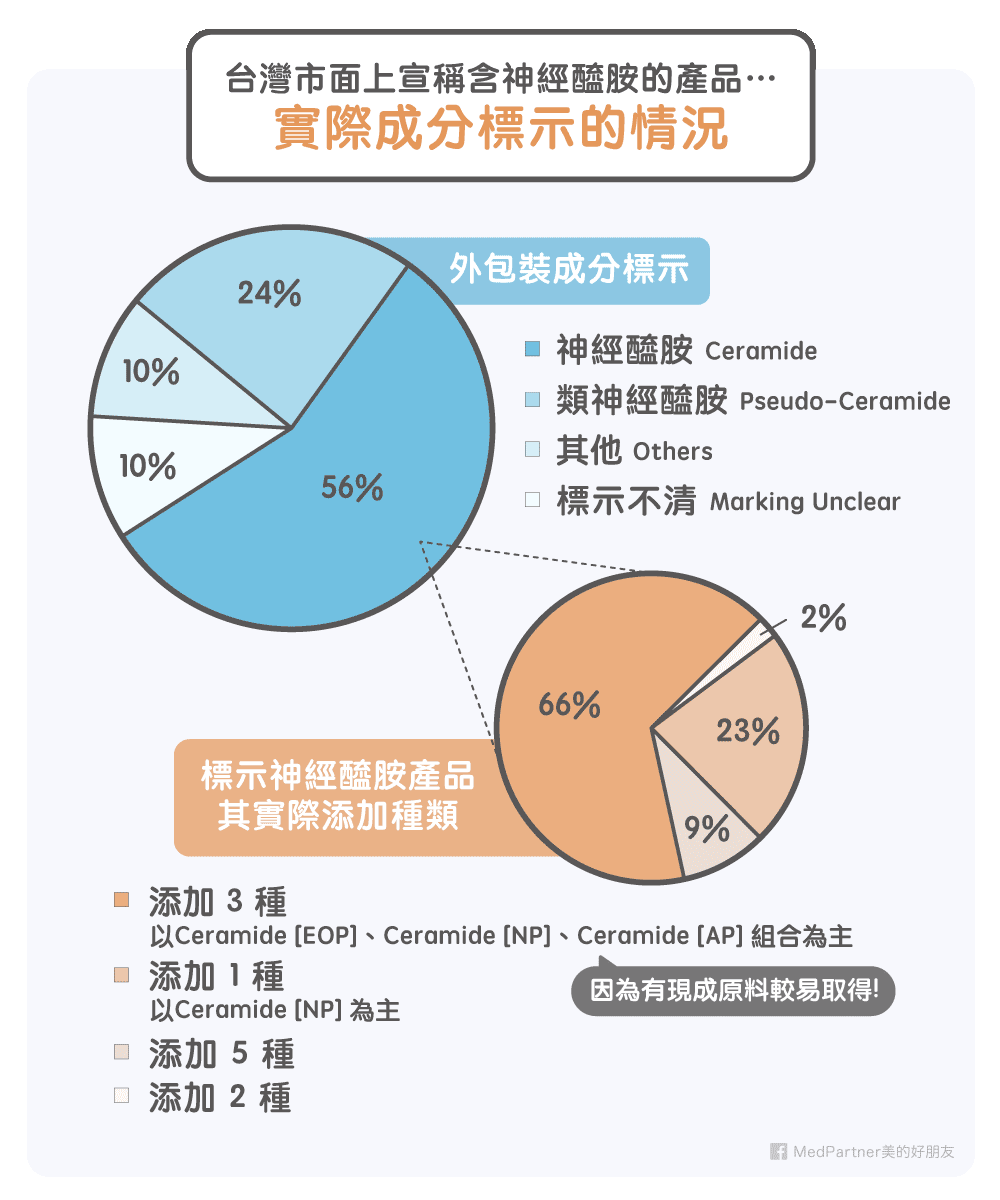
MedPartner 團隊調查了市面上 79 種包裝或廣告標示以神經醯胺為添加物的產品,包含了精華液、乳液(霜)、眼(晚)霜、防曬乳、面膜。根據其外包裝的成分列表做出了一個整理。其中 56% 為神經醯胺添加,24% 為類神經醯胺,10% 表示為 Sphingolipids、Glycosphingolipids 等非神經醯胺或類神經醯胺的脂類成分。標示不清的占約 10%,主要的原因是某些產品只標示 “Ceramide” 這樣的非 INCI 命名而不完整披露使用何種神經醯胺。含神經醯胺的產品中以添加 3種佔 66% 最多,這 3 種組合以 Ceramide [EOP]、Ceramide [NP]、Ceramide [AP] 為主,主要的原因是因為原料上有現成的原料可以添加。只加入一種神經醯胺的也有 23%,以 Ceramide [NP] 為主。如果您從上文已經了解到神經醯胺在皮膚的複雜性,就會知道只補充一類的神經醯胺可能是不足的。
講了這麼多讓人頭痛的科學與醫學知識,那消費者究竟該如何選擇神經醯胺保養品呢?我們在現有的證據下,提出以下建議:
- 消費者可考慮使用含神經醯胺/類神經醯胺的產品,特別是濕疹相關疾病患者可能較有幫助。但要注意其中的配方是否合理,以含仿角質層脂質(膽固醇、脂肪酸)的成分組成較為理想。(但這類的產品的問題是,最佳濃度、最佳比例、整體產品的劑型與成分間的交互作用難以評估。特定產品對皮膚受損或某些皮膚疾病患者的幫助,仍需進一步的研究。)
- 對於有嚴重皮膚疾病的消費者,使用含神經醯胺/類神經醯胺的產品可能減緩症狀,但是否建議使用這類保養品,建議諮詢專業皮膚科醫師。
- 神經醯胺是成本較高的生理性脂質,並非每個人都缺乏。以價錢的考量上,若是皮膚狀況正常的消費者,未必要選用含神經醯胺的產品。若您使用其他產品,仍無法做到預期的保濕功效,或皮膚症狀無法緩解時,在醫師的評估與建議後,再選用含神經醯胺/類神經醯胺的保養品即可。
另外在現實狀況下有個問題是,除非是醫師有參與開發過程或實驗過程,或廠商提供了相關實驗數據並提供足夠樣品讓醫師給患者測試,不然醫師實在很難單從成份表判斷這類產品的功效,民眾也難以簡單從成份表找到適合的選擇。期待國內外廠商有使用相關成份的話,可朝多與醫師合作進行相關研究,或提供足量的試用品,這樣醫師才能有信心推薦這類的產品給適合的民眾啊。
Reference
- Elias, P.M. “Epidermal barrier function: intercellular lamellar lipid structures, origin, composition and metabolism.” Journal of Controlled Release 15, 199–208 (1991).
- Iwai, I. et al. “The human skin barrier is organized as stacked bilayers of fully extended ceramides with cholesterol molecules associated with the ceramide sphingoid moiety.” Journal of Investigative Dermatology 132, 2215–2225 (2012).
- Moore, D. J. and Rawlings, A. V. “The chemistry, function and (patho)physiology of stratum corneum barrier ceramides.” International Journal of Cosmetic Science 39, 366–372 (2017).
- Bergfeld, W. F. et al. “Safety assessment of ceramides as used in cosmetics.” Cosmetic Ingredient Review. May 16, 2014.
- t’Kindt, R. et al. “Profiling and characterizing skin ceramides using reversed-phase liquid chromatography-quadrupole time-of-flight mass spectrometry.” Analytical Chemistry 84, 403–411 (2012).
- van Smeden, J. et al. “Combined LC/MS-platform for analysis of all major stratum corneum lipids, and the profiling of skin substitutes.” Biochimica et Biophysica Acta 1841, 70–79 (2014).
- Rogers, J. et al. “Stratum corneum lipids: the effect of ageing and the seasons.” Archives of Dermatological Research 288, 765–770 (1996).
- Tfayli, A. et al. “Raman spectroscopy: feasibility of in vivo survey of stratum corneum lipids, effect of natural aging.” European Journal of Dermatology: EJD 22, 36–41 (2012).
- Kihara A. “Synthesis and degradation pathways, functions, and pathology of ceramides and epidermal acylceramides.” Progress in Lipid Research 63, 50–69 (2016).
- Huang, H. C. et al. “Ceramide 1 and ceramide 3 act synergistically on skin hydration and the transepidermal water loss of sodium lauryl sulfate-irritated skin.” The International Society of Dermatology 47, 812–819 (2008).
- Chamlin, S. L. et al. “Ceramide-dominant barrier repair lipids alleviate childhood atopic dermatitis: Changes in barrier function provide a sensitive indicator of disease activity.” Journal of the American Academy of Dermatology 47, 198–208 (2002).
- Imokawa, G. et al. “Selective recovery of deranged water-holding properties by stratum corneum lipids.” Journal of Investigative Dermatology 87, 758–761 (1986).
- Zettersten E. M. et al. “Optimal ratios of topical stratum corneum lipids improve barrier recovery in chronologically aged skin.” Journal of the American Academy of Dermatology 37, 403–408 (1997).
- Paepe, K. D. et al. “Blackwell Science, Ltd Incorporation of ceramide 3B in dermatocosmetic emulsions: effect on the transepidermal water loss of sodium lauryl sulphatedamaged skin.” Journal of the European Academy of Dermatology and Venereology 14, 272–279 (2000).
- Berardesca, E. et al. “Evaluation of efficacy of a skin lipid mixture in patients with irritant contact dermatitis, allergic contact dermatitis or atopic dermatitis: a multicenter study.” Contact Dermatitis 45, 280–285 (2001).
- Paepe, K. D. et al. “Repair of acetone- and sodium lauryl sulphate-damaged human skin barrier function using topically applied emulsions containing barrier lipids.” Journal of the European Academy of Dermatology and Venereology 16, 587–594 (2002).
- Park, W. S. et al. “Improvement of skin barrier function using lipid mixture.” SOFW Journal 127, 10–18 (2001).
- Mizutani, H. et al. The Nishinihon Journal of Dermatology 63, 457–461 (2001).
- Nakamura, T. et al. The Nishinihon Journal of Dermatology 61, 671–681 (1999).
- Chamlin, S. L. et al. “Ceramide-dominant barrier repair lipids alleviate childhood atopic dermatitis: changes in barrier function provide a sensitive indicator of disease activity.” Journal of the American Academy of Dermatology 47, 198–208 (2002).
- Lee, E. J. et al. “The clinical efficacy of a multi-lamellar emulsion containing pseudoceramide in childhood atopic dermatitis: an open crossover study.” Annals of Dermatology 15, 133–138 (2003).
- Simpson, E. et al. “Safety and tolerability of a body wash and moisturizer when applied to infants and toddlers with a history of atopic dermatitis: results from an open-label study.” Pediatric Dermatology 29, 590–597 (2012).
- Kim, D. S. et al. “Delayed ERK activation by ceramide reduces melanin synthesis in human melanocytes.” Cellular Signaling 14, 779–785 (2002).